《细胞》:给坏细胞指定死路!科学家开发可稳定诱导细胞焦亡的方法,全新的抗癌、抗衰、抗感染方法有望诞生
来源:奇点糕 2024-04-30 09:41
想要干掉细胞,其实不难,但对于死法,细胞很有“自己的想法”。
加州理工大学团队在《细胞》杂志发文,研究者们利用合成生物学开发了可诱导特定细胞凋亡/焦亡的蛋白质回路synpoptosis,可在不同环境中有条件地激活或抑制靶细胞的细胞凋亡和焦亡,还可以此为基础设计杀伤性细胞。
synpoptosis不仅可用于杀死癌细胞,衰老细胞、纤维化细胞、自靶向免疫细胞、受感染的宿主细胞等有害细胞都可以成为synpoptosis的靶细胞,这也意味着它有无穷的发展潜力。
论文题图
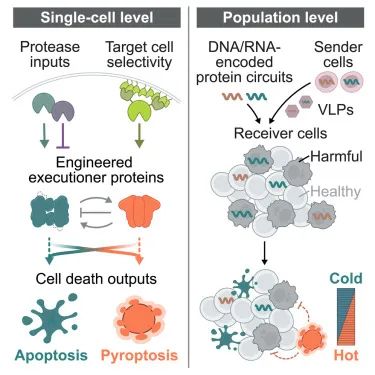
想要干掉细胞,其实不难,但对于死法,细胞很有“自己的想法”。
例如,当细胞毒性淋巴细胞将颗粒酶递送到靶细胞时,缺乏GSDM的靶细胞会发生细胞凋亡,而表达GSDM的靶细胞则会焦亡。也就是说,死亡诱导剂是决定不了细胞以什么方式去世的。
研究者比对了凋亡和焦亡过程,发现蛋白酶是个很好的着手点。凋亡过程中,半胱天冬酶(caspases)会激活促凋亡因子,焦亡中,半胱天冬酶也会裂解GSDM以形成焦亡孔。而且本来合成生物学就很擅长利用蛋白酶搞事,这不是正好吗。
研究者选择的是对caspase-3有修饰能力的烟草蚀刻病毒蛋白酶(TEVP)。研究者设计了增添活性基团的caspase-3变体,使其在基团不被TEVP切割的情况下活性显著降低,通过TEVP有否实现了对细胞凋亡的控制。
同理,研究者设计了GSDM变体控制细胞焦亡。
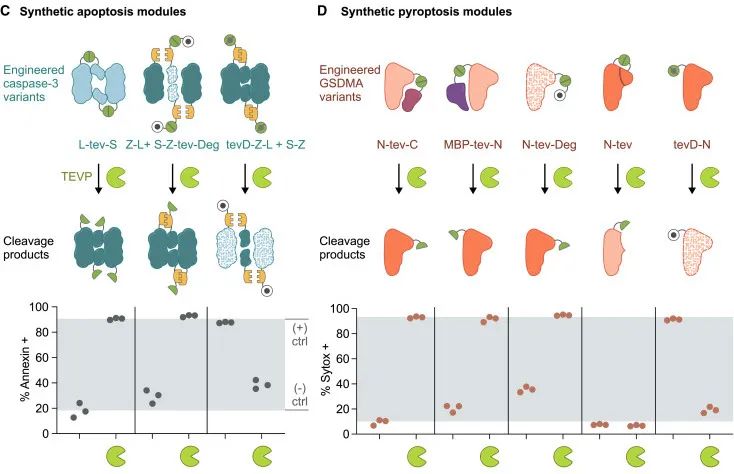
Annexin高表示细胞凋亡;Sytox高表示细胞焦亡
当然,单纯让细胞凋亡或焦亡不是我们的目的,让想凋亡的细胞焦亡,让想焦亡的细胞凋亡才算完成控制。
有趣的是,在同时表达TEVP激活的caspase-3变体和GSDM变体的情况下,细胞会从凋亡转向焦亡,看起来选择死法这事儿上GSDM更胜一筹。
给细胞添加caspase-3天然底物GSDME,GSDME本身不会诱导细胞死亡,但会被TEVP激活的caspase-3变体激活,将细胞引向焦亡。
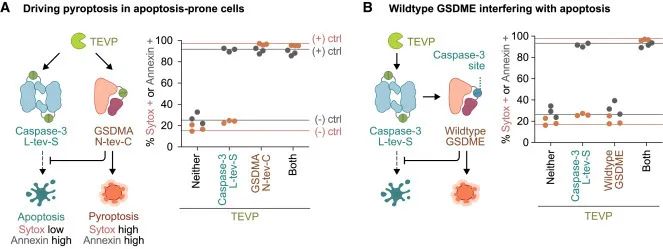
GSDME一步将凋亡变焦亡
通过抑制剂调节GSDME活性,研究者实现了细胞凋亡和细胞焦亡的平衡。端水还得靠滴定啊。
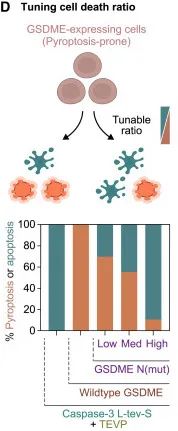
滴定抑制剂调节细胞凋亡和焦亡比例
不用说,回路的开关研究者们也做了,不过这段没有提及应用的具体条件,就是做了一下与或非门,咱们看个图速速跳过。
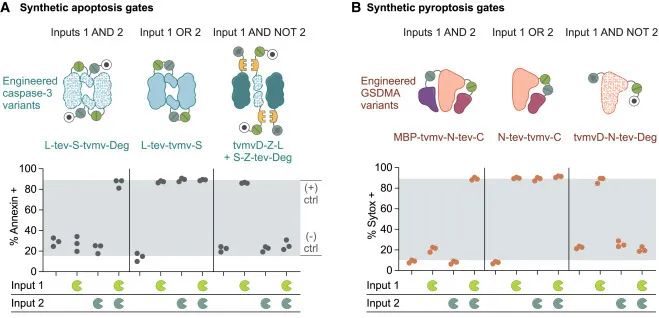
启动回路的组合条件设计
那么如何寻找靶细胞呢?
研究者选择的实验目标是Ras癌基因。他们将TEVP的非活性N端和C端分别设计与Ras融合,当活性Ras存在的时候,TEVP的两个半边就能重聚成有修饰功能的TEVP,完成下游一系列操作。
从实验结果来看,预期还是达成得蛮好。
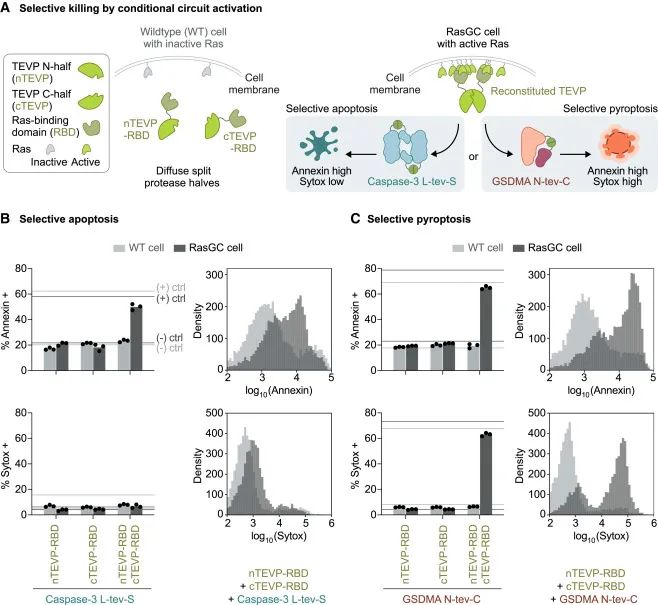
可识别表达活性HRas-G12V的HEK(RasGC)
最后,研究者尝试利用细胞递送synpoptosis,使用工程化的发送细胞释放含有synpoptosis的病毒样颗粒(VLP)。为了不让发送细胞先死于synpoptosis,研究者将回路拆分成两个部分分别发送,给组件添加膜定位序列则能够提升组件之间的拼接效率。
这可以用于生产装载synpoptosis的职业细胞杀手。

细胞递送的思路
不过这项研究还是比较基础的,仅能控制凋亡和焦亡两种细胞死亡方式,实验也都在永生细胞系中进行,天然细胞环境中是否能正常生效还未可知。本项研究也仅限于哺乳动物细胞,如果能用于细菌或真菌,指不定也可以开发新型抗生素啊。
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


